| Disulfan | |
|---|---|
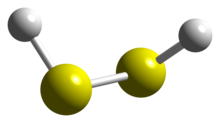
 Vazby v disulfanu | |
| Obecné | |
| Systematický název | disulfan |
| Triviální název | persulfid vodíku |
| Ostatní názvy | dithioperoxid vodíku |
| Anglický název | Hydrogen disulfide |
| Sumární vzorec | H2S2 |
| Vzhled | žlutá kapalina |
| Identifikace | |
| Registrační číslo CAS | 13465-07-1 |
| PubChem | 108196 |
| SMILES | H-S-S-H |
| InChI | InChI=1/H2S2/c1-2/h1-2H |
| Vlastnosti | |
| Molární hmotnost | 66,136 g/mol |
| Teplota tání | −89,6 °C |
| Teplota varu | 70,7 °C |
| Hustota | 2,95 g/cm3 (0 °C, 101,325 kPa, plyn) |
Některá data mohou pocházet z datové položky. | |
Disulfan je jedna ze sloučenin síry s vodíkem, její vzorec je H2S2.Jeho vodný roztok se nazývá kyselina disulfanová a její soli hydrogendisulfidy a disulfidy, například disulfid železnatý, který se v přírodě vyskytuje jako pyrit a markazit.
Vzniká mimo jiné nahrazením obou atomů kyslíku v molekule peroxidu vodíku atomy síry:
H2O2 + 2S → H2S2 + O2
nebo rozkladem sulfanu:
2 H2S → H2S2 + H2
nebo z methylmerkaptanu:
2 CH3SH → H2S2 + C2H6.
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu Disulfan na Wikimedia Commons
Obrázky, zvuky či videa k tématu Disulfan na Wikimedia Commons
 |
Tento článek je příliš stručný nebo postrádá důležité informace. Pomozte Wikipedii tím, že jej vhodně rozšíříte. Nevkládejte však bez oprávnění cizí texty. |
| Zdroj dat | cs.wikipedia.org |
|---|---|
| Originál | cs.wikipedia.org/wiki/Disulfan |


